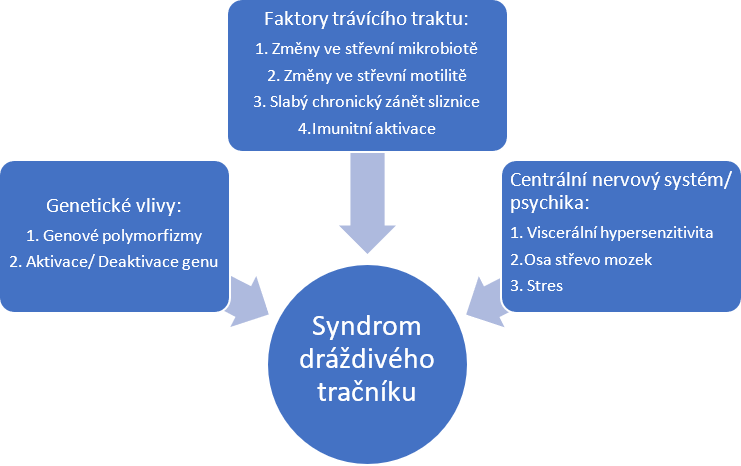
IBS se dělí na podskupiny dle převládajícího způsobu vyprazdňování, protože od toho se odvíjí následná terapie. To znamená, že IBS je různorodé onemocnění a je pravděpodobné, že u každé podskupiny IBS jsou dominantní jiné příčiny vzniku. Ze začátku se výzkum zaměřoval hlavně na změny ve střevní motilitě a viscerální senzorické funkce, které jsou určitě důležité pro vysvětlení mechanismu onemocnění. Ale poslední dobu se výzkum posouvá více k objasnění, proč a jak vůbec tyto změny vznikají. Zkoumají se role různých příčin jako je vztah osy střevo-mozek (psychika), genetické faktory, infekce, změny ve střevní mikroflóře, abnormality v metabolismu serotoninu, zánět střeva, imunitní aktivace, změna v propustnosti střeva, změny v metabolismu žlučových kyselin, vliv diety atd.
Osa mozek-střevo
U pacientů trpících IBS je vyšší výskyt hlavně úzkosti a deprese. To vedlo k tomu, že dlouho dobu se IBS bral jako primární porucha funkce mezi mozkem a střevem, dokonce až jako somatizace psychických obtíži (porucha v psychice je příčinou gastrointestinálních a ostatních projevů)1. V novějších populačních studiích IBS se objevují i data, které poukazují na to, že vztah psychiky a střeva při IBS je obousměrný, a že u přibližně poloviny pacientů se nejprve objevují funkční střevní potíže a psychické poruchy se vytvoří až později 2,3. Proto je u této skupiny pacientu šance, že správné zaléčení syndromu dráždivého střeva zlepší i poruchy psychiky.
Na druhé straně u zbývající části pacientů, kteří trpí psychickými obtížemi, právě tyto obtíže předcházely vzniku IBS. Na základě epidemiologických dat je možno vidět například u lidí s historii týraní nebo zneužívaní v dětství vyšší výskyt IBS ve srovnání s běžnou populací. Další studie poukazují nato, že u těchto lidí se může vyskytovat přehnaná reakce nervového systému v trávicím traktu na běžné podněty.
Proto je správné předpokládat, že tento vztah je obousměrný s tím, že u části pacientů může být prvotní spouštěč psychika a u jiné části je to jenom důsledek IBS.
Genetické faktory
Stále více různých genetických polymorfismů se spájí se syndromem dráždivého tračníku. Některé geny související s imunitní regulací, funkcí epiteliální bariéry, syntézy žlučových kyselin, kanabinoidních receptorů atd. mohou zvyšovat šanci vzniku IBS4. Předpokládá se, že vliv na vznik onemocnění má i aktivace a deaktivace různých genů během života.
Infekce a změna střevní mikroflóry
Hlavně u průjmové formy syndromu dráždivého tračníku je možné dopátrat střevní infekci před samotným objevením symptomů IBS. Proto se začíná tato forma nazývat i Postinfekční syndrom dráždivého střeva (PI-IBS). Výskyt PI-IBS po střevní infekci se odhaduje přibližně na 10 % 5. Nejvyšší riziko pro vývoj představuje infekce parazitem Giardia lambialis, případně jinými protozoemi6. Pravděpodobně při tomto typu IBS po infekci přetrvává slabý chronický zánět ve střevní sliznici, který postupně spouští kaskádu změn.
Často můžeme u pacientů s IBS pozorovat změny ve střevní mikroflóře ve smyslu dysbiózy (snížený počet prospěšných baktérií a zároveň zvýšený počet patogenních baktérií), menší různorodosti baktérií atd. Například množství a aktivita Laktobaktérii a Bifidobaktérii (prospěšné kmeny baktérii) je u IBS výrazně menší 7.
Změna v metabolismu žlučových kyselin
U části pacientů hlavně u průjmové formy syndromu dráždivého střeva se vyskytuje změna v metabolismu žlučových kyselin, a to ve formě zvýšeného množství žlučových kyselin ve stolici. Může to být způsobené nadprodukcí těchto kyselin, nebo špatnou zpětní resorpci ve střevě a následně nadbytek kyselin urychluje střevní průchod.
Samozřejmě to nejsou všechny faktory, které se podílejí na rozvoji syndromu dráždivého střeva. U každé skupiny pacientu poměr vlivů je jiný. Proto syndrom dráždivého tračníku z hlediska příčin vzniku není jedno onemocnění, ale je to skupina onemocnění, která má podobné projevy.
1 Tanaka Y, Kanazawa M, Fukudo S, Drossman DA. Biopsychosocial model of irritable bowel syndrome. J Neurogastroenterol Motil 2011; 17: 131–39.
2 Wessely S, Nimnuan C, Sharpe M. Functional somatic syndromes: one or many? Lancet 1999; 354: 936–39.
3 Koloski NA, Jones M, Kalantar J, Weltman M, Zaguirre J, Talley NJ. The brain-gut pathway in functional gastrointestinal disorders is bidirectional: a 12-year prospective population-based study. Gut 2012; 61: 1284–90.
4 Chong PP, Chin VK, Looi CY, Wong WF, Madhavan P and Yong VC (2019) The Microbiome and Irritable Bowel Syndrome – A Review on the Pathophysiology, Current Research and Future Therapy. Front. Microbiol. 10:1136. doi: 10.3389/fmicb.2019.01136
5 Klem, Fabiane, et al. "Prevalence, risk factors, and outcomes of irritable bowel syndrome after infectious enteritis: a systematic review and meta-analysis." Gastroenterology 152.5 (2017): 1042-1054.
6 Wensaas KA, Langeland N, Hanevik K, et al. Irritable bowel syndrome and chronic fatigue 3 years after acute giardiasis: historic cohort study. Gut 2012;61:214-9.
7 Bellini, M., Gambaccini, D., Stasi, C., Urbano, M. T., Marchi, S., and Usai-Satta, P. (2014). Irritable bowel syndrome: a disease still searching for pathogenesis, diagnosis and therapy. World J. Gastroenterol. 20, 8807–8820. doi: 10.3748/wjg.v20.i27.8807
Holtmann, Gerald J., Alexander C. Ford, and Nicholas J. Talley. "Pathophysiology of irritable bowel syndrome." The lancet Gastroenterology & hepatology 1.2 (2016): 133-146.